能量守能。
- 物体内能的增加等于物体吸收的热量和对物体所作的功的总和.
- 系统在绝热状态时,功只取决于系统初始状态和结束状态的能量,和过程无关。
- 孤立系统的能量永远守恒。
- 系统经过绝热循环,其所做的功为零,因此第一类永动机是不可能的(即不消耗能量做功的机械)。
- 两个系统相互作用时,功具有唯一的数值,可以为正、负或零。
热能只能从热到冷变化。不能自发的逆向发生。
热力学第三定律:
熵只能从低到高变化。不能自发逆向发生。
永动机:
第一类永动机:机械装置自发运动。
如魔轮。
被热力学第一定律禁止。即不存在”不消耗能量做功的机械“。
第二类永动机:能量装置自发运动。
历史上首个成型的第二类永动机装置是1881年美国人约翰·嘎姆吉为美国海军设计的零发动机,这一装置利用海水的热量将液氨汽化,推动机械运转。但是这一装置无法持续运转,因为汽化后的液氨在没有低温热源存在的条件下无法重新液化,因而不能完成循环。
被热力学第二定律禁止。
熵
熵的概念是由德國物理學家克勞修斯於1865年所提出。克氏定義一個熱力學系統中熵的增減:在一個可逆性程序裡,被用在恆溫的熱的總數(δQ),並可以公式表示為:
克勞修斯對變數S予以「熵」(希臘語:εντροπια,entropia,德語:Entropie,英語:entropy)一名,希臘語源意為「內向」,亦即「一個系統不受外部干擾時往內部最穩定狀態發展的特性」。
事物最原始的状态(即最无序的状态),熵最高。
熱力學中熵表示的是「系統混亂狀態」;信息論中信息熵表示的是信息量;生態學中熵表示的是生物多樣性。
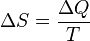
没有评论:
发表评论